Dit is een vertaling van deze pagina.
Lees ook eens DIT artikel.
“Bad ass” nieuwe methode gebruikt een gemagnetiseerd eiwit om hersencellen snel, omkeerbaar en niet-invasief te activeren
Onderzoekers in de Verenigde Staten hebben een nieuwe methode ontwikkeld voor het aansturen van de hersencircuits die samenhangen met complex diergedrag. Ze gebruiken genetische manipulatie om een gemagnetiseerd eiwit te creëren dat specifieke groepen zenuwcellen op afstand activeert.
Begrijpen hoe de hersenen gedrag genereren, is een van de ultieme doelen van de neurowetenschap – en een van de moeilijkste vragen. In de afgelopen jaren hebben onderzoekers een aantal methoden ontwikkeld waarmee ze bepaalde groepen neuronen op afstand kunnen besturen en de werking van neuronale circuits kunnen onderzoeken.
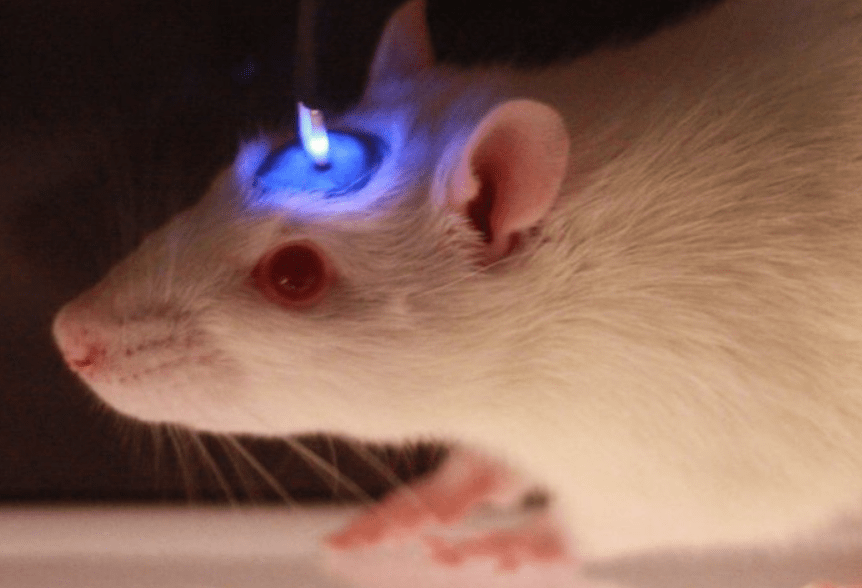
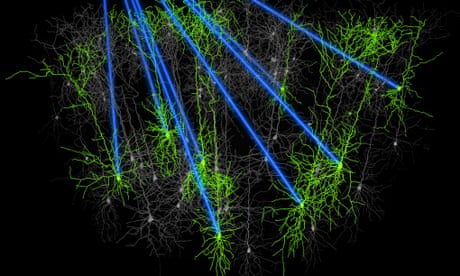
De krachtigste hiervan is een methode die optogenetica wordt genoemd , waarmee onderzoekers populaties van verwante neuronen kunnen in- of uitschakelen op een tijdschaal van milliseconde per milliseconde met pulsen van laserlicht. Een andere recent ontwikkelde methode, chemogenetica genaamd , maakt gebruik van gemanipuleerde eiwitten die worden geactiveerd door designergeneesmiddelen en kunnen worden gericht op specifieke celtypen.
Hoewel krachtig, hebben beide methoden nadelen. Optogenetica is invasief en vereist het inbrengen van optische vezels die de lichtpulsen in de hersenen afgeven en bovendien is de mate waarin het licht het dichte hersenweefsel binnendringt, ernstig beperkt. Chemogenetische benaderingen overwinnen beide beperkingen, maar induceren doorgaans biochemische reacties die enkele seconden duren om zenuwcellen te activeren.
De nieuwe techniek, ontwikkeld in het laboratorium van Ali Güler aan de Universiteit van Virginia in Charlottesville, en beschreven in een voorafgaande online publicatie in het tijdschrift Nature Neuroscience , is niet alleen niet-invasief, maar kan ook neuronen snel en omkeerbaar activeren.
Verschillende eerdere onderzoeken hebben aangetoond dat zenuwceleiwitten die worden geactiveerd door hitte en mechanische druk genetisch kunnen worden gemanipuleerd zodat ze gevoelig worden voor radiogolven en magnetische velden , door ze te hechten aan een ijzeropslaand eiwit dat ferritine wordt genoemd, of aan anorganische paramagnetische deeltjes . Deze methoden zijn een belangrijke stap vooruit – ze worden bijvoorbeeld al gebruikt om de bloedsuikerspiegel bij muizen te reguleren – maar bevatten meerdere componenten die afzonderlijk moeten worden geïntroduceerd.
De nieuwe techniek bouwt voort op dit eerdere werk en is gebaseerd op een eiwit genaamd TRPV4, dat gevoelig is voor zowel temperatuur als rekkrachten . Deze stimuli openen de centrale porie, waardoor elektrische stroom door het celmembraan kan stromen; dit roept zenuwimpulsen op die in het ruggenmerg en vervolgens naar de hersenen reizen.
Güler en zijn collega’s redeneerden dat magnetische torsie (of roterende) krachten TRPV4 zouden kunnen activeren door de centrale porie open te trekken, en daarom gebruikten ze genetische manipulatie om het eiwit te fuseren met het paramagnetische gebied van ferritine, samen met korte DNA-sequenties die cellen signaleren om te transporteren eiwitten naar het zenuwcelmembraan en steek ze erin.
https://www.youtube-nocookie.com/embed/iHTpJNSNFlc?wmode=opaque&feature=oembedIn vivo manipulatie van het gedrag van zebravissen met Magneto. Zebravislarven vertonen oprolgedrag als reactie op gelokaliseerde magnetische velden. Van Wheeler et al (2016).
Toen ze dit genetische construct introduceerden in menselijke embryonale niercellen die in petrischalen groeiden, synthetiseerden de cellen het ‘Magneto’-eiwit en stopten het in hun membraan. Toepassing van een magnetisch veld activeerde het gemanipuleerde TRPV1-eiwit, zoals blijkt uit tijdelijke verhogingen van de calciumionconcentratie in de cellen, die werden gedetecteerd met een fluorescentiemicroscoop.
Vervolgens plaatsten de onderzoekers de Magneto-DNA-sequentie in het genoom van een virus, samen met het gen dat codeert voor groen fluorescerend eiwit, en regulerende DNA-sequenties die ervoor zorgen dat het construct alleen tot expressie wordt gebracht in specifieke soorten neuronen. Vervolgens injecteerden ze het virus in de hersenen van muizen, gericht op de entorhinale cortex, en ontleedden de hersenen van de dieren om de cellen te identificeren die groene fluorescentie uitstraalden. Met behulp van micro-elektroden toonden ze vervolgens aan dat het toepassen van een magnetisch veld op de hersenschijfjes Magneto activeerde, zodat de cellen zenuwimpulsen produceren.
Om te bepalen of Magneto kan worden gebruikt om neuronale activiteit bij levende dieren te manipuleren, injecteerden ze Magneto in zebravislarven, gericht op neuronen in de romp en staart die normaal een ontsnappingsreactie regelen. Vervolgens plaatsten ze de zebravislarven in een speciaal gebouwd gemagnetiseerd aquarium en ontdekten dat blootstelling aan een magnetisch veld kronkelende manoeuvres veroorzaakte die vergelijkbaar waren met die tijdens de ontsnappingsreactie. (Bij dit experiment waren in totaal negen zebravislarven betrokken, en daaropvolgende analyses onthulden dat elke larve ongeveer 5 neuronen bevatte die Magneto tot expressie brengen.)
In een laatste experiment injecteerden de onderzoekers Magneto in het striatum van vrij gedragende muizen, een diepe hersenstructuur die dopamine-producerende neuronen bevat die betrokken zijn bij beloning en motivatie, en plaatsten de dieren vervolgens in een apparaat dat was opgesplitst in gemagnetiseerde en niet-gemagnetiseerde secties. . Muizen die Magneto tot expressie brachten, brachten veel meer tijd door in de gemagnetiseerde gebieden dan muizen die dat niet deden, omdat activering van het eiwit ervoor zorgde dat de striatale neuronen die het tot expressie brachten dopamine vrijgaven, zodat de muizen vonden dat ze in die gebieden lonend waren. Dit toont aan dat Magneto het afvuren van neuronen diep in de hersenen op afstand kan regelen en ook complex gedrag kan beheersen.
Neurowetenschapper Steve Ramirez van Harvard University, die optogenetica gebruikt om herinneringen in de hersenen van muizen te manipuleren, zegt dat de studie ” badass ” is.
“Eerdere pogingen [met behulp van magneten om neuronale activiteit te regelen] hadden meerdere componenten nodig om het systeem te laten werken – magnetische deeltjes injecteren, een virus injecteren dat een warmtegevoelig kanaal uitdrukt, [of] het dier vastzetten zodat een spoel veranderingen kan veroorzaken in magnetisme”, legt hij uit. “Het probleem met een systeem met meerdere componenten is dat er zoveel ruimte is voor elk afzonderlijk stuk om af te breken.”
“Dit systeem is een enkel, elegant virus dat overal in de hersenen kan worden geïnjecteerd, waardoor het technisch gemakkelijker en minder waarschijnlijk is dat bewegende toeters en bellen kapot gaan”, voegt hij eraan toe, “en hun gedragsapparatuur is slim ontworpen om magneten te bevatten waar nodig, zodat de dieren vrij kunnen bewegen.”
‘Magnetogenetica’ is daarom een belangrijke aanvulling op de gereedschapskist van neurowetenschappers, die ongetwijfeld verder zal worden ontwikkeld, en biedt onderzoekers nieuwe manieren om hersenontwikkeling en -functie te bestuderen.
Referentie
Wheeler, MA, et al . (2016). Genetisch gerichte magnetische controle van het zenuwstelsel. nat. Neurowetenschappen , DOI: 10.1038/nn.4265 [ Samenvatting ]





